
노인성 치매의 가장 흔한 원인으로 알려진 알츠하이머병은 전 세계 GDP의 1%를 차지할 정도로 사회, 경제적 소모비용이 큰 질환입니다. 하지만 여전히 알츠하이머병을 일으키는 분자 유전학적 원인은 명확하게 규명되지 않고 있죠. 기존의 알츠하이머병 유전체 연구는 주로 환자의 말초조직인 혈액에서 전장유전체 연관분석(Genome-wide association study)을 하거나, APP, PSEN1/2와 같이 이미 가족력이 있는 환자에서 발견된 일부 유전자들에 대한 유전자 패널 분석 등이 주를 이루었는데요.
KAIST 의과학대학원 이정호 교수, KISTI 국가슈퍼컴퓨팅본부 유석종 박사 공동 연구팀이 노화 과정에서 발생하는 후천적 뇌 돌연변이가 알츠하이머병의 새 원인이 될 수 있다는 이론을 제시했다고 합니다. <Nature Communications>에 게재된 논문에 따르면 연구팀은 52명의 알츠하이머병 환자에게 얻은 사후 뇌 조직에서 데이터 분석을 통해 알츠하이머병에 존재하는 뇌 체성 유전변이를 찾아냈다고 합니다. 뿐만 아니라 뇌 체성 돌연변이가 알츠하이머병의 중요 원인으로 알려진 신경섬유다발 형성을 비정상적으로 증가시킴을 확인했다고 합니다.
어떻게 연구했는가
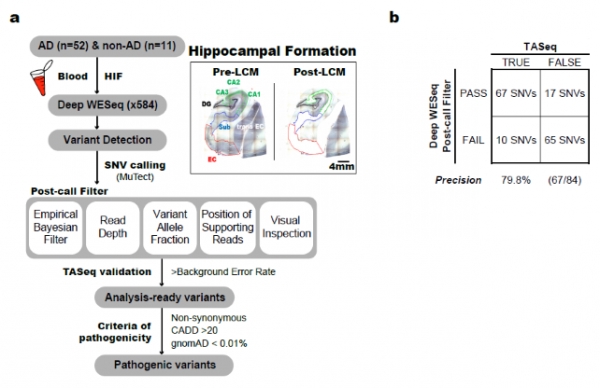
연구팀은 신경섬유다발이 처음 나타나는 내후각피질(Entorhinal cortex)을 포함한 주변 해마 형성체에 누적된 체성 유전변이가 알츠하이머병 발병에 기여했다는 가설을 바탕으로 알츠하이머병 환자 및 대조군의 해마 형성체 조직을 레이저 현미 해부법을 통해 수확했습니다. 그 다음 연구팀은 500X 이상의 고심도 엑솜 시퀀싱(Deep whole exome sequencing)을 시행했는데요. 연구팀은 생성된 전장 엑솜 유전체 빅데이터의 생명정보학 분석을 이용해 알츠하이머병 환자와 정상인의 뇌에서 나타나는 체성 유전변이를 분석했습니다.

유전체 분석 결과 알츠하이머 환자와 정상인 사이에서 뇌 및 혈액의 평균 체성 유전변이 수, 대립 유전자 빈도 및 유전변이 종류에는 유의미한 차이가 없었다고 합니다. 연구팀은 알츠하이머 환자의 뇌 및 혈액 모두에서 체성 유전변이가 환자의 사망 연령에 따라 선형 증가하지만, 누적 속도는 혈액 조직에서 4.8배 빠르게 나타남을 확인했습니다. 이어서 돌연변이원(Mutation Signature)을 분석 결과 연구팀은 22.2%의 알츠하이머 뇌 체성 유전변이는 과활성 산소에 의한 DNA 손상에 의한 것으로 나타난다는 것을 발견했습니다.
또한 연구팀은 26.9%의 알츠하이머 환자의 뇌에서는 병원성 체성 유전변이들(Pathogenic brain somatic mutation)이 타우 단백질의 과-인산화와 관련된 PI3K-AKT, MAPK, AMPK 경로에 유의하게 누적되어 있음을 확인했습니다.

마지막으로 연구팀은 알츠하이머 환자의 뇌에서 나타난 PIN1 유전자의 병원성 체성 유전변이를 시험관 내에서의 녹다운 실험을 통해 모방했을 때 타우 단백질의 과-인산화와 올리고머화가 증가함을 확인했습니다. 연구 결과를 통해 연구팀은 알츠하이머 환자의 해마 형성체 내에 누적된 체성 유전변이의 일부가 타우 단백질의 과-인산화를 통해 알츠하이머 발병에 기여할 수 있다는 결론을 내렸습니다.
앞으로의 전망

이정호 교수와 연구를 함께한 KISTI 유석종 박사는 "연구팀이 구축한 저빈도 체성 유전변이 분석 파이프라인 및 빅데이터 분석을 위한 슈퍼컴퓨팅 기술을 통해 알츠하이머병의 새로운 발병 원리를 밝혀냈다"라며 "타 유전체 기반 연구에 활용할 수 있는 기반을 마련했다"라고 말했습니다.
##참고자료##

